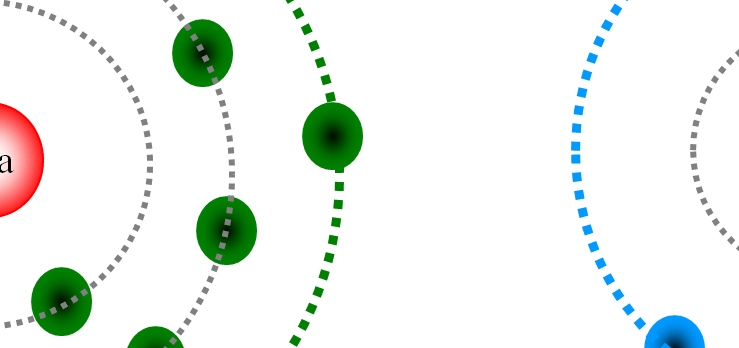
أمرت إلكترونات مجالات الطاقة الأولى والثانية والثالثة لذرة الصوديوم للإلكترون بالعديد من الخصائص المهمة التي ظهرت بعد عدة دراسات وتجارب وأبحاث. سنقوم بتلخيصها لك ببضعة أسطر ، لأنها مهمة لدراسة الكيمياء في موضوعنا. تنظيم الإلكترونات من مجالات الطاقة الأولى والثانية والثالثة لذرة الصوديوم.
تنظيم إلكترونات مجال الطاقة الأول والثاني والثالث لذرة الصوديوم
- التقييم. تندرج تحت نموذج فيزياء الجسيمات.
- وزنه 9.109 × 10-31 كجم.
- الإلكترون يمكن أن يكون موجات.
- الإلكترونات هي أجسام متناظرة.
- لديها هيئات افتراضية.
- العنصر النشط الذي يولد الطاقة في الحقول هو عنصر جذاب للجسم.
يضع الإلكترونات في مجالات الطاقة الأولى والثانية والثالثة.
أي كائن مع واحد أو أكثر من الإلكترونات هو موصل للكهرباء ، لأن الإلكترون يحمل شحنة موجبة ، وبفضل دراستنا للإلكترون ، عندما تكون سرعته مساوية لسرعة الضوء ، تزداد الكتلة النسبية ، وهذه الكميات هي عناصر مهمة للذرة.
الإلكترونيات هي أشياء مهمة في الحياة لأنها تدخل في العديد من الظواهر الفيزيائية ، بما في ذلك الموصلية الكهربائية أو الكهرباء ، فهي جسم متحرك يولده مجال مغناطيسي ، لأنه في مجال المغناطيس يتم استخدام الإلكترون لأنه قادر على إنتاج أو امتصاص الطاقة.
P / وضع الطاقة الأولى والثانية والثالثة من المجال الإلكتروني لذرة الصوديوم؟
الإجابة على السؤال:
- أولا ن = 1 2x (1 × 2) = 2.
- الثانية ن = 2 2x (2 × 2) = 8.
- الثالث ن = 3 2 س (3 × 3) = 18.
- الرابع ن = 4 2 س (4 س 4) = 32.
في ختام موضوعنا حول الإلكترونات ، أحد العناصر المهمة التي تتشكل في الذرة ، اكتشف العلماء أن العنصر يحمل شحنة كهربائية مماثلة لشحنة البروتون ، تماما كما ننظم إلكترونات حقول الطاقة الأولى والثانية والثالثة لذرة الصوديوم.
